【内审员培训】《GB/T42061-2022/ISO13485:2016 内审员》培训通知
 序言
序言
国家市场监督管理总局/国家标准化管理委员会于2022年10月12日发布了GB/T 42061-2022《医疗器械 质量管理体系 用于法规的要求》,并将于2023年11月1日正式实施。该要求是原YY/T 0287-2017在贯彻落实相关质量管理的法律法规基础上,为进一步提升医疗器械全生命周期的实施影响力,升级成为了国家标准。这有力凸显了质量管理体系在行业监管中的重要性。
自2021年6月1日新版《医疗器械监督管理条例》实施以来,药监部门陆续发布了一系列新的医疗器械法规,结合国内各类生产企业产品备案/注册、日常监督、飞行检查必须执行/落实的《医疗器械生产质量管理规范》和特定产品“附录”,动态系统地为医疗器械行业及其供应链相关参与方持续健康发展提供技术支撑。
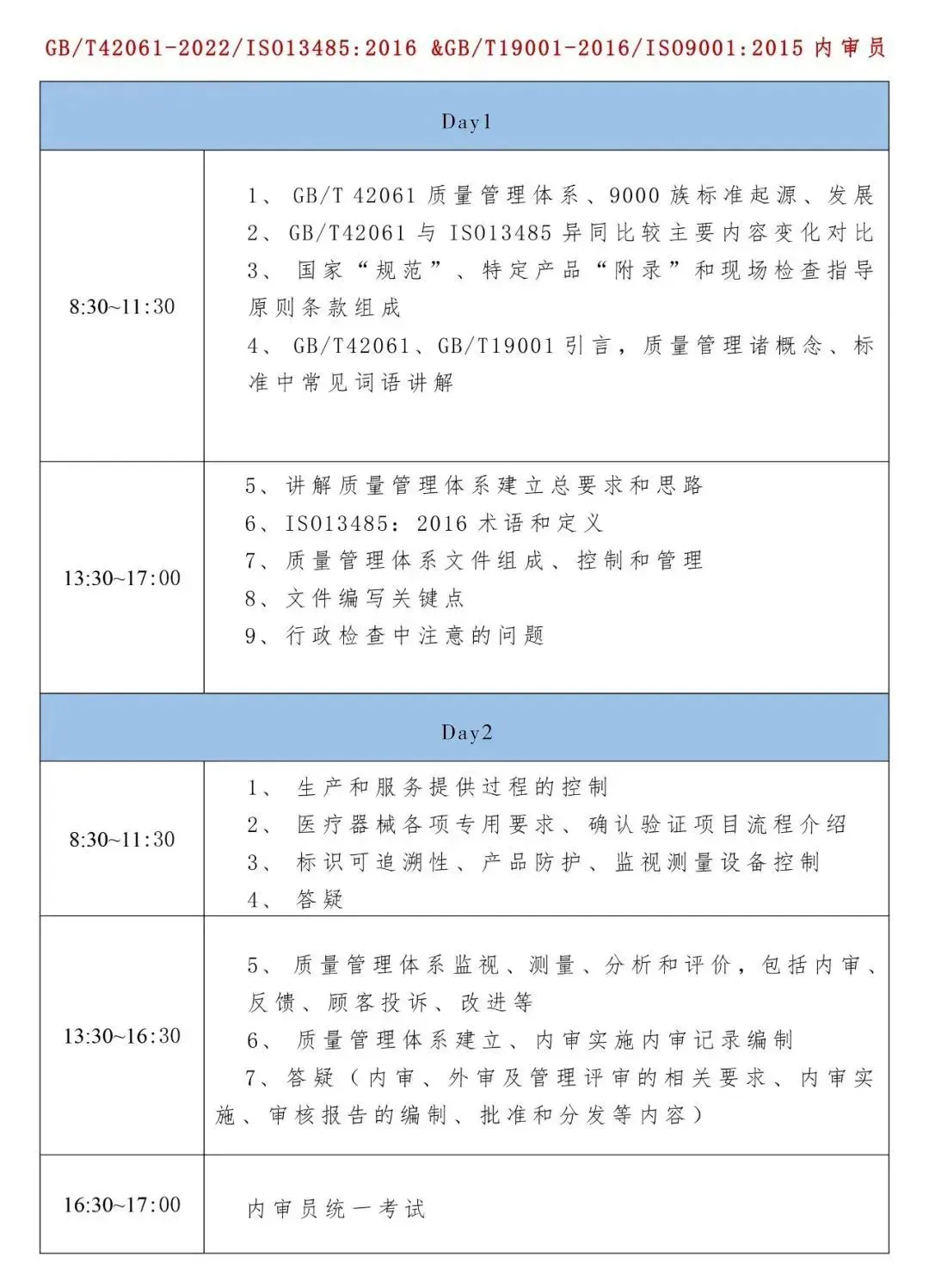
为使企业充分理解和落实“标准”和“规范”要求、协助质量管理体系顺利升级,以适应国家行政检查和第三方认证检查,解决企业在实际操作中遇到的问题,常州飞凡实训中心特举办《GB/T 42061-2022/ISO 13485:2016 & GB/T 19001-2016/ISO 9001:2015内审员》转版培训课程。
顾朋超老师
医疗器械体系审核专家
三体系外审员
12年体系审核经验
毕业于南京航空航天大学,机械自动化专业本科,至今工作12年,涉及骨科、外科无菌手术器械、康复器材等多领域医疗器械的研发及体系辅导、审核工作。
/ 报名方式 /
请扫码报名,场地有限先报先得

扫描上方二维码报名参加培训
考核通过后领取培训证书
(培训信息可查询)
培训费用及缴费方式
培训费用:
非会员2500元/人 会员1800元/人
缴费方式:
账户:常州飞凡医药信息咨询服务有限公司
开户行:中国银行股份有限公司常州湖塘支行
账号:5222 5977 2281
近期内审员培训计划
▶ 2023年4月14日-4月15日
▶ 2023年6月9日-6月10日
▶ 2023年8月11日-8月12日
▶ 2023年10月13日-10月14日
▶ 2023年12月14日-12月15日

培训材料

联系人



